Senyawa-senyawa kovalen dengan ikatan kimia dengan kovalen nonpolar maka tidak ada muatan parsial baik positif maupum negatif. Senyawa anorganik merupakan konduktor kuat dibandingkan dengan senyawa.

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube
Konduktivitas arus listrik mengalirkan arusnya tergantung pada mobilitas ion dan kadar yang terlarut.

. Kelarutan dalam pelarut nonpolar. Perbedaan Kunci - Senyawa Ionic vs Covalent. Perbandingan beberapa sifat senyawa kovalen dan ion.
Jelaskan Perbedaan Antara Senyawa Ion Dan Kovalen Polar Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya. Oleh karena itu pola ikatan dapat dianggap sebagai. Pelarut organik merupakan senyawa karbon misalnya bensin minyak tanah alkohol dan aseton.
Molekul Penyusun Keterangan Ikatan HCl Gas Gas 2 atom tidak sejenis. Senyawa kovalen nonpolar timbul karena perbedaan elektronegativitas antaratom yang sangat kecil bahkan hampir sama. Senyawa kovalen tidak larut dalam pelarut polar namun larut dalam pelarut organik.
No Senyawa kovalen Senyawa ion 1 Kebanyakan menunjukkan titik Kebanyakan menunjukkan titik leleh rendah. Perbedaan Utama Senyawa Kovalen Polar Dengan Senyawa Ionik Sifat fisis senyawa ion umumnya berbeda dengan senyawa kovalen. Sifat sifat Fisika.
Home Layout 1. Senyawa kovalen memiliki ikatan kovalen. Senyawa kovalen terbagi menjadi senyawa kovalen polar dan senyawa kovalen nonpolar.
Ikatan Kovalen Polar dan Non Polar a Ikatan Kovalen Polar terjadi jika dua atom non logam berbeda kelektronegatifannya berikatan maka pasangan elektron ikatan akan lebih tertarik ke atom yang lebih elektronegatif. Sifat sifat fisika senyawa ion dan kovalen. Senyawa kovalen polar hanya dapat menghantarkan listrik dalam larutan dan senyawa kovalen nonpolar tidak dapat menghantarkan listrik.
Senyawa kovalen berwujud lunak dan tidak mudah rapuh. Alasan utama perbedaan ini adalah perbedaan dalam pola ikatan mereka. Pada senyawa ionik elektron diberikan dari atom dari satu unsur ke unsur lainnya.
Senyawa ion juga lebih larut dalam air dibandingkan senyawa kovalen. Home Layout 2. 16030654057 UNIVERSITAS NEGERI SURABAYA JURUSAN IPA 20162017 FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM 1 Bab I Pendahuluan 11 Latar.
Karakter kovalen hidrida menurun dan karakter ioniknya meningkat. Di antara senyawa berikut yang bukan molekul kovalen polar adalah. Hal ini karena air melarutkan zat polar yang merupakan konsistensi senyawa ionik sedangkan senyawa kovalen non-polar.
Ikatan kovalen terjadi akibat penggunaan bersama-sama pasangan elektron oleh dua atom. Ikatan O-H dalam air dan ikatan Cl-H. Dianggap polar dan berdisosiasi di air menghasilkan H.
Karena PEI tertarik sama kuat maka bentuk molekul pada senyawa F 2 adalah simetris. Senyawa kovalen tidak dapat menghantarkan listrik. Polar Kovalen polar NaCl Logam Gas Ion NH3 Gas Gas PEI 3 N golongan V A PEB 5 3 2 Kovalen polar H2O Gas Gas PEI 2 O golongan.
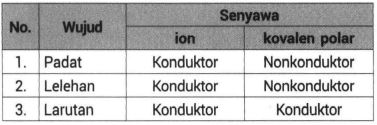
Pada senyawa kovalen di samping itu elektron bersama oleh. Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas. Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya.
Pada suhu kamar berbentuk gas ada juga yang berwujud cair dan padat. HF asam florida. Leleh tinggi 350oC sering sampai 1000oC.
SEORANG PENGGUNA TELAH BERTANYA Jelaskan perbedaan antara senyawa kovalen dan senyawa ion serta berikan contohnya. Senyawa kovalen memiliki titik didih dan titik leleh yang rendah. Senyawa kovalen tidak memiliki kemampuan ini karena mereka tidak mengandung ion.
Berikut merupakan tabel perbedaan senyawa ion dan senyawa kovalen. Memiliki titik didih dan titik leleh yang relatif rendah. Sifat-sifat senyawa kovalen adalah.
2 Umumnya cairan atau gas pada Semuanya dalah padatan pada suhu. Perbandingan sifat senyawa kovalen dan senyawa ion. Senyawa ionik terbentuk oleh transfer elektron yang bermuatan.
Terbentuknya senyawa BF3 NH3 5. Oleh sebab itu larutan yang bersumber dari senyawa ionik dapat menghantarkan arus listrik dengan baik dan termasuk ke dalam larutan elektrolit kuat. Sementara itu senyawa kovalen polar timbul karena perbedaan elektronegativitas yang cukup besar antara dua atom.
Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas. Untuk lebih memahami materi ini silahkan anda. Home Layout 3.
Hal ini disebabkan oleh cara pembentu. Senyawa kovalen polar memiliki perbedaan keelektronegatifan besar antar atom sehingga ada gaya tarik menarik yang dapat memutuskan ikatanikatan dalam molekul. Hal ini terjadi karena antara dua atom F dan F memiliki keelektronegatifan yang sama besar atau perbedaan elektronegativitas adalah nol.
Namun ada beberapa senyawa kovalen yang dapat larut dalam air karena terjadi reaksi dengan air hidrasi dan membentuk ion-ion. LAPORAN RESMI KIMIA SENYAWA ION DAN SENYAWA KOVALEN Oleh Kelompok 10. Senyawa ion memiliki ikatan ion dalam bentuk lelehan dan larutan dapat terionisasi sempurna menghasilkan ion-ion yang dapat bergerak bebas.
Apabila senyawanya terionisasi sempurna maka akan dihasilkan larutan elektrolit kuat sedangkan bila senyawanya terionisasi sebagian maka akan dihasilkan larutan elektrolit lemah. Senyawa kovalen polar dalam bentuk larutannya dapat terionisasi sempurna atau terionisasi sebagian menjadi ion-ionnya sehingga dapat menghantarkan arus listrik. Banyak perbedaan dapat dicatat antara senyawa ionik dan kovalen berdasarkan sifat makroskopisnya seperti kelarutan dalam air konduktivitas listrik titik leleh dan titik didih.
Dalam kimia senyawa ionik adalah senyawa kimia yang tersusun dari ion-ion yang disatukan oleh gaya elektrostatik yang disebut ikatan ionikSenyawa ini netral secara keseluruhan tetapi terdiri dari ion bermuatan positif yang disebut kation dan ion bermuatan negatif yang disebut anionMasing-masing ion bisa berupa ion sederhana seperti natrium Na dan klorida Cl. Tolong jawabannya ya makasihh INI JAWABAN TERBAIK Perbedaan senyawa ion dan senyawa kovalen. Oleh karena itu ikatan kovalen polar lebih mudah putus daripada ikatan kovalen nonpolar.
Deya Hetri Safira 16030654022 Annisa Aura Lelyani 16030654028 Febrina Hanif Addaafi 16030654041 Karennina Putri A. Misalnya asam sulfat bila dilarutkan ke dalam air akan membentuk ion hidrogen dan ion sulfat.
![]()
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen

Sebutkan Sifat Atau Ciri Senyawa Kovalen Dan Ion Brainly Co Id

Perbedaan Senyawa Ion Senyawa Kovalen Dan Logam Utakatikotak Com
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po
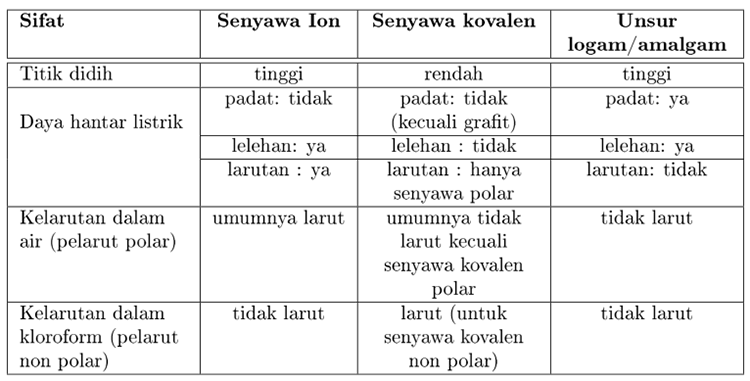
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College
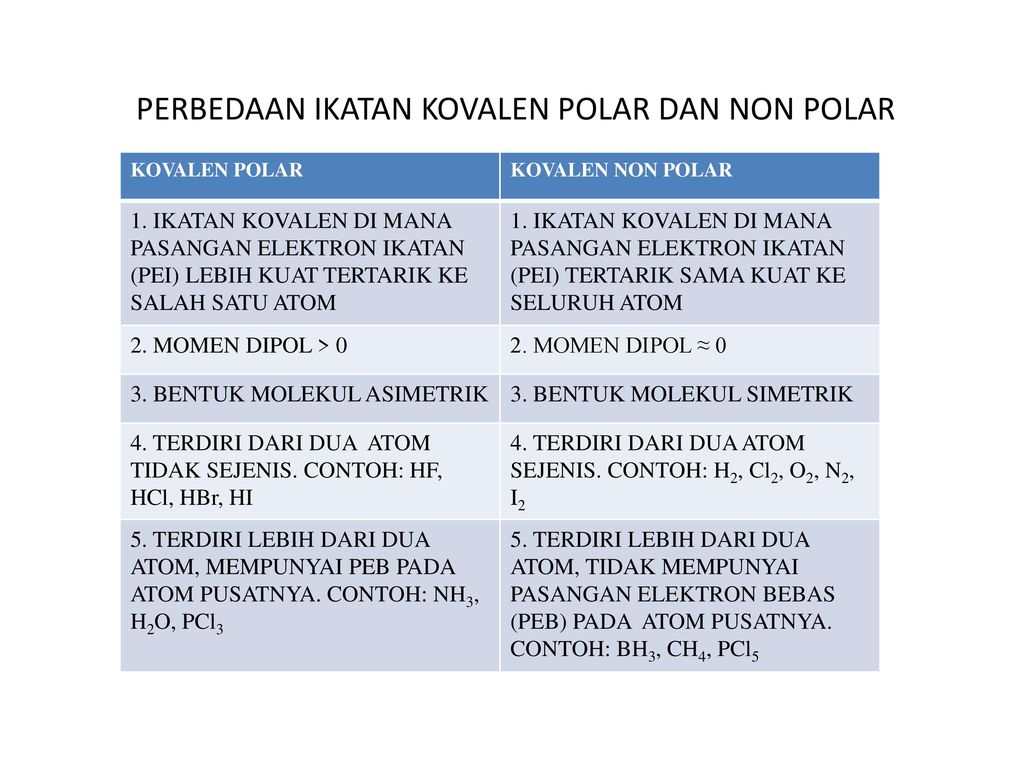
Perbedaan Ikatan Kovalen Polar Dan Non Polar Ppt Download

Pengertian Sifat Dan Contoh Dari Senyawa Ion Panduan Kimia Riset

Ciri Ciri Dari Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Buat Yang Kelas 10 Yuk Mengenal Ikatan Ikatan Kimia Dalam Atom

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection
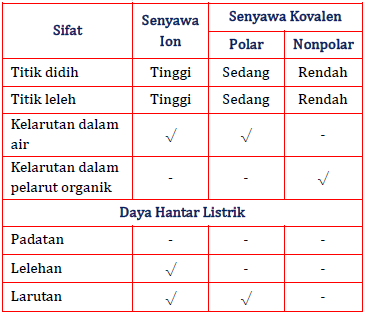
Diketahui Data Fisik Dua Buah Senyawa Sebagai Beri

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube

Sebutkan Perbedaan Sifat Antara Senyawa Ion Dengan Senyawa Kovalen Brainly Co Id

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya

Sebutkan 5 Contoh Perbedaan Antara Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Sebutkan 8 Perbedaan Senyawa Polar Dan Nonpolar Konsep Pentingnya Usaha Tiga Dua Satu

